今年央视3.15晚会,第二弹就是曝光了郑州一家“三无体检队”,无资质、无医学背景、无认证,由一家销售角膜塑形镜的科视视医院医院组织,入郑州、开封、焦作等城市的几百所中小学进行体检,要求体检的孩子填写“视力异常登记表”获取其个人信息,截止到目前已获得条学生信息。
说到医疗机构验配角膜塑形镜的规定,早在年原卫生部和国家食药监管局就发过相关规范性文件。
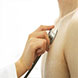
上图源自网络
卫生部关于加强医疗机构验配角膜塑形镜管理的通知
角膜塑形镜(俗称OK镜)是一种通过与眼球直接接触,改变角膜形态来矫治屈光不正的医疗器械。近一段时间以来,患者在使用角膜塑形镜过程中出现不良反应的情况时有发生,有的甚至因此造成了严重后果。为保证医疗安全,维护患者权益,现就医疗机构验配角膜塑形镜的执业管理提出以下要求:一、验配角膜塑形镜的基本条件(一)医疗机构1、具有《医疗机构执业许可证》;2、二级(含二级)以上的医疗机构;3、医疗机构执业登记的诊疗科目中有眼科;4、有接待室、检查室、验光室和配戴室等,并有良好的卫生条件。(二)人员1、医师(1)具有执业医师资格;(2)具有中级以上眼科医师职称;(3)参加省级卫生行政部门或省级卫生行政部门委托专业学术团体组织的相关知识培训并经考核合格者。2、技师(1)具有中级以上技师职称;(2)参加省级卫生行政部门或省级卫生行政部门委托专业学术团体组织的相关知识培训并经考核合格者。符合验配基本条件技师必须在眼科医生的配合下完成验配OK镜的工作。(三)设备具备角膜曲率计、角膜地形图仪(8mm以上直径测量范围)、非接触眼压计、角膜厚度测定仪、电脑验光仪、综合验光仪、验光试片箱、裂隙灯显微镜、远/近视力表、检眼镜、眼底镜、荧光素钠试纸、焦度计、镜片投影仪(不低于7.5倍)、镜片弧度测定仪等。二、操作规范(一)验配前,验配人员必须真实、客观地向患者告知角膜塑形镜的各项性能、可能出现的不良反应和副作用、验配程序等,并取得就医者的签字同意。(二)根据检查数据确定是否适合配戴角膜塑形镜,除眼科裂隙灯常规检查外,应包括:角膜形态、角膜厚度、眼轴、眼压、眼位、远/近视力、屈光度、泪液测试、角膜直径、瞳孔直径、眼底检查。(三)首次配戴镜片和定配前应进行试戴,观察、评估适配状态。(四)根据检查数据和试戴评估结果设计定片参数和配戴方案。(五)为患者提供角膜塑形镜使用指导,将指导内容以“使用说明书”的形式发放给每位患者。(六)建立并严格执行复诊制度,复诊的时间是初戴OK镜后两天内、和戴镜后一周、一个月、二个月、三个月之后随诊。三、各级卫生行政部门要按照《医疗机构管理条例》中关于设置或变更诊疗科目的有关规定,根据上述要求认真做好本辖区内医疗机构开展此项诊疗活动的日常监管工作。对本辖区内业已开展此项诊疗活动的医疗机构按照上述要求进行清理整顿,并将执行过程中出现的有关情况及时报送我部。
二OO一年八月十七日
关于印发角膜塑形用硬性透气接触镜说明书编写指导原则的通知
食药监办械函[]号
各有关单位:
为进一步加强角膜塑形用硬性透气接触镜(俗称OK镜,以下简称角膜塑形镜)的管理,国家食品药品监督管理局组织制定了《角膜塑形用硬性透气接触镜说明书编写指导原则》,现予印发,并将有关实施要求通知如下:
一、角膜塑形镜应当在符合《卫生部关于加强医疗机构验配角膜塑形镜管理的通知》(卫医发〔〕号)规定的医疗机构验配。
二、自本指导原则发布之日起,申请注册角膜塑形镜产品,生产企业应当提交根据本指导原则编写的中文说明书;境外产品还应提交产品在境外上市所使用的正式说明书及翻译件。
三、已经受理,尚未完成审批的产品,由医疗器械技术审评机构通知生产企业补充根据本指导原则编写的说明书。
四、已取得医疗器械注册证的产品,生产企业应当根据本指导原则修改说明书,并于本指导原则发布之日起一个月内按照说明书备案要求,履行说明书备案手续。境外产品还应同时提交产品在境外上市所使用的正式说明书及翻译件。自年6月1日起,所有销售使用的塑形镜产品都应配有经重新备案的产品说明书。
附件:角膜塑形用硬性透气接触镜说明书编写指原则导
国家食品药品监督管理局办公室
二○一一年四月十一日
相关链接:
3?15晚会曝光了这些食药黑幕,涉及这些公司
3?15晚会遭啪啪打脸?被曝光企业:食品合法,不下架!
3・15晚会曝光食品问题后,食药总局这样回应~
3?15必知!生活中这些都是“霸王条款”!
3?15,食药总局公布10批次不合格药品!
食药法苑
食药企业及监管者的资讯新媒体
预览时标签不可点收录于话题#个上一篇下一篇



 当前时间:
当前时间:  E-Mail:
E-Mail: